

Unsere Forschung
Überblick über unsere drei Forschungsschwerpunkte:
- a. Identifizierung von sog. „elite neutralizers“ bei HCV-Infektionen und Etablierung eines HCV-permissiven Tiermodells zur Unterstützung der Entwicklung eines HCV-Impfstoffs. Der HCV-Impfstoff wird mit Hilfe einer Multi-Plattform-Strategie entwickelt.
- b. Identifizierung von genetischen Varianten und/oder quantitativer Biomarker, die das Risiko und die Schwere des RSV-Krankheitsverlaufs in ansonsten gesunden Säuglingen ohne Vorerkrankungen vorhersagen können. Darüber hinaus nutzen wir Substanzbibliotheken, um neue Zielstrukturen für Medikamente gegen RSV zu identifizieren.
- c. Screening mehrerer Bibliotheken mit zugelassenen oder in der Entwicklung weit fortgeschrittenen Medikamenten sowie von neu identifizierten kleinen Molekülen zur Entdeckung von antiviralen Wirkstoffen, die auf den Wirt abzielen. Letztendlich wollen wir im Hinblick auf die Pandemievorsorge antivirale Wirkstoffe gegen Coronaviren mit breitem Wirkungsspektrum identifizieren.
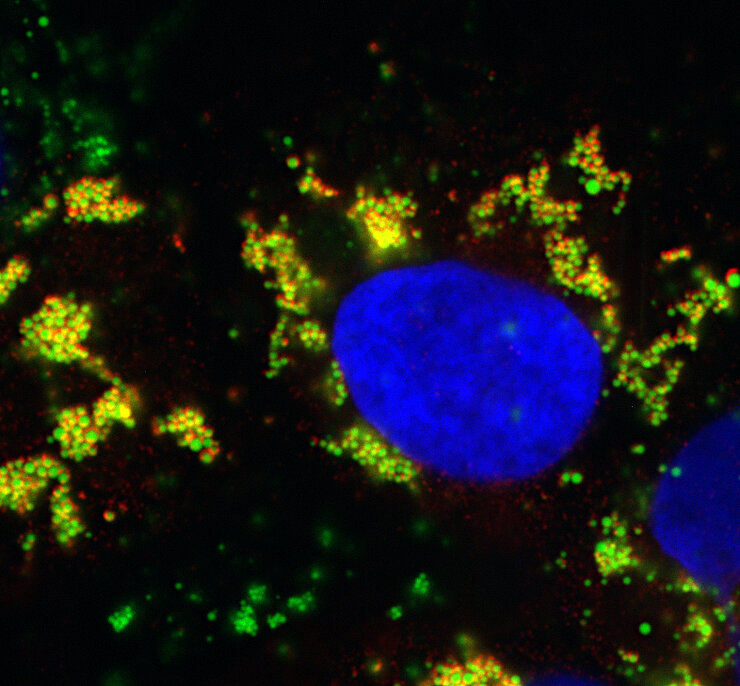
Hepatitis C-Virus (HCV)
Nach Schätzungen der Weltgesundheitsorganisation (WHO) sind rund 58 Millionen Menschen chronisch mit dem Hepatitis-C-Virus (HCV) infiziert. Als Folge der chronischen Infektion entwickeln viele Patienten eine Leberentzündung (Hepatitis), die die Funktion des Organs beeinträchtigen und zu einer Leberfibrose, -zirrhose und -krebs führen kann. Glücklicherweise ist die chronische Hepatitis C heute mit einer Kombinationstherapie gut behandelbar. Dennoch bleiben große Herausforderungen bestehen: Die große Mehrheit der HCV-Infektionen wird nicht diagnostiziert und bleibt unentdeckt. Darüber hinaus schützt eine medikamentöse Heilung nicht vor einer erneuten Infektion mit HCV. Zusätzlich bleibt die Virustransmission mit mehr als 1,5 Millionen Neuinfektionen pro Jahr hoch. Daher ist die Entwicklung eines prophylaktischen Impfstoffs zur Begrenzung der Virusübertragung und zur Sicherung des Behandlungserfolgs nach wie vor von entscheidender Bedeutung.
Wir erforschen die Prinzipien, die für den Immunschutz gegen HCV verantwortlich sind, wobei wir uns vor allem auf Antikörper-vermittelte Mechanismen konzentrieren. Wir untersuchen dabei Strategien, mit denen Viren eine Immunantwort umgehen, und entwickeln Zellkultur- und Tiermodelle, um die Wirksamkeit von Impfstoffkandidaten zu testen. Diese Systeme werden genutzt, um einen Impfstoffkandidaten zu entwickeln.
Respiratorisches Synzytial-Virus (RSV)
Das Respiratorische Synzytial-Virus (RSV) ist ebenso wie HCV weltweit verbreitet. Bei jungen, gesunden Erwachsenen äußert sich eine RSV-Infektion in der Regel in Form einer leichten Erkältung. RSV kann jedoch auch schwere Infektionen der unteren Atemwege verursachen. Besonders gefährdet sind kleine Kinder, immungeschwächte Patienten wie z. B. Transplantatempfänger und Ältere über 60 Jahre. Weltweit verursacht RSV allein bei Kleinkindern 33,4 Millionen Fälle von akuten Infektionen der unteren Atemwege und zwischen 53.000 und 199.000 damit verbundene Todesfälle pro Jahr. Warum manche Kinder besonders schwere Krankheitsverläufe entwickeln, ist nicht genau bekannt. Derzeit gibt es nur wenige Behandlungsmöglichkeiten und nur zwei Impfstoffe zum Schutz von Personen ab 60 Jahren vor RSV-bedingten Erkrankungen sind zugelassen.
Unsere Forschung konzentriert sich auf die Prinzipien, die für schwere RSV-Infektionen bei Kleinkindern verantwortlich sind. Ziel dabei ist die Entwicklung von Diagnosemethoden, um diese besonders anfällige Gruppe besser zu schützen. Darüber hinaus erforschen wir direkte antivirale Substanzen gegen RSV.
Pandemic Preparedness
Bis Mitte 2023 hat der Erreger der COVID-19-Pandemie, SARS-CoV-2, fast 7 Millionen Menschen weltweit getötet. Obwohl mehrere Impfstoffe verfügbar sind, gibt es nur wenige Behandlungsmöglichkeiten für COVID-19. Im Hinblick auf die Pandemievorsorge gehen wir davon aus, dass in Zukunft auch andere Coronaviren auf den Menschen übertragen werden. Daher entwickeln wir antivirale Moleküle, die gegen eine Vielzahl verschiedener Coronaviren wirksam sind.
Ausführliche Informationen über aktuelle Projekte der Forschungsgruppe Experimentelle Virologie finden Sie auf der TWINCORE-Website.
Unsere Forschung
Überblick über unsere drei Forschungsschwerpunkte:
- a. Identifizierung von sog. „elite neutralizers“ bei HCV-Infektionen und Etablierung eines HCV-permissiven Tiermodells zur Unterstützung der Entwicklung eines HCV-Impfstoffs. Der HCV-Impfstoff wird mit Hilfe einer Multi-Plattform-Strategie entwickelt.
- b. Identifizierung von genetischen Varianten und/oder quantitativer Biomarker, die das Risiko und die Schwere des RSV-Krankheitsverlaufs in ansonsten gesunden Säuglingen ohne Vorerkrankungen vorhersagen können. Darüber hinaus nutzen wir Substanzbibliotheken, um neue Zielstrukturen für Medikamente gegen RSV zu identifizieren.
- c. Screening mehrerer Bibliotheken mit zugelassenen oder in der Entwicklung weit fortgeschrittenen Medikamenten sowie von neu identifizierten kleinen Molekülen zur Entdeckung von antiviralen Wirkstoffen, die auf den Wirt abzielen. Letztendlich wollen wir im Hinblick auf die Pandemievorsorge antivirale Wirkstoffe gegen Coronaviren mit breitem Wirkungsspektrum identifizieren.

Hepatitis C-Virus (HCV)
Nach Schätzungen der Weltgesundheitsorganisation (WHO) sind rund 58 Millionen Menschen chronisch mit dem Hepatitis-C-Virus (HCV) infiziert. Als Folge der chronischen Infektion entwickeln viele Patienten eine Leberentzündung (Hepatitis), die die Funktion des Organs beeinträchtigen und zu einer Leberfibrose, -zirrhose und -krebs führen kann. Glücklicherweise ist die chronische Hepatitis C heute mit einer Kombinationstherapie gut behandelbar. Dennoch bleiben große Herausforderungen bestehen: Die große Mehrheit der HCV-Infektionen wird nicht diagnostiziert und bleibt unentdeckt. Darüber hinaus schützt eine medikamentöse Heilung nicht vor einer erneuten Infektion mit HCV. Zusätzlich bleibt die Virustransmission mit mehr als 1,5 Millionen Neuinfektionen pro Jahr hoch. Daher ist die Entwicklung eines prophylaktischen Impfstoffs zur Begrenzung der Virusübertragung und zur Sicherung des Behandlungserfolgs nach wie vor von entscheidender Bedeutung.
Wir erforschen die Prinzipien, die für den Immunschutz gegen HCV verantwortlich sind, wobei wir uns vor allem auf Antikörper-vermittelte Mechanismen konzentrieren. Wir untersuchen dabei Strategien, mit denen Viren eine Immunantwort umgehen, und entwickeln Zellkultur- und Tiermodelle, um die Wirksamkeit von Impfstoffkandidaten zu testen. Diese Systeme werden genutzt, um einen Impfstoffkandidaten zu entwickeln.
Respiratorisches Synzytial-Virus (RSV)
Das Respiratorische Synzytial-Virus (RSV) ist ebenso wie HCV weltweit verbreitet. Bei jungen, gesunden Erwachsenen äußert sich eine RSV-Infektion in der Regel in Form einer leichten Erkältung. RSV kann jedoch auch schwere Infektionen der unteren Atemwege verursachen. Besonders gefährdet sind kleine Kinder, immungeschwächte Patienten wie z. B. Transplantatempfänger und Ältere über 60 Jahre. Weltweit verursacht RSV allein bei Kleinkindern 33,4 Millionen Fälle von akuten Infektionen der unteren Atemwege und zwischen 53.000 und 199.000 damit verbundene Todesfälle pro Jahr. Warum manche Kinder besonders schwere Krankheitsverläufe entwickeln, ist nicht genau bekannt. Derzeit gibt es nur wenige Behandlungsmöglichkeiten und nur zwei Impfstoffe zum Schutz von Personen ab 60 Jahren vor RSV-bedingten Erkrankungen sind zugelassen.
Unsere Forschung konzentriert sich auf die Prinzipien, die für schwere RSV-Infektionen bei Kleinkindern verantwortlich sind. Ziel dabei ist die Entwicklung von Diagnosemethoden, um diese besonders anfällige Gruppe besser zu schützen. Darüber hinaus erforschen wir direkte antivirale Substanzen gegen RSV.
Pandemic Preparedness
Bis Mitte 2023 hat der Erreger der COVID-19-Pandemie, SARS-CoV-2, fast 7 Millionen Menschen weltweit getötet. Obwohl mehrere Impfstoffe verfügbar sind, gibt es nur wenige Behandlungsmöglichkeiten für COVID-19. Im Hinblick auf die Pandemievorsorge gehen wir davon aus, dass in Zukunft auch andere Coronaviren auf den Menschen übertragen werden. Daher entwickeln wir antivirale Moleküle, die gegen eine Vielzahl verschiedener Coronaviren wirksam sind.
Ausführliche Informationen über aktuelle Projekte der Forschungsgruppe Experimentelle Virologie finden Sie auf der TWINCORE-Website.
Prof. Dr. Thomas Pietschmann
Wir untersuchen auf molekularer Ebene die Hintergründe für das klinische Erscheinungsbild von Viruserkrankungen wie HCV oder RSV und schlagen damit eine Brücke zwischen Klinik und Grundlagenforschung.

Der gebürtige Würzburger Thomas Pietschmann studierte Biologie an der Justus-Maximilian-Universität Würzburg und der Duke University, Durham USA. Im Jahr 2000 promovierte er am Institut für Virologie der Universität Würzburg über Mechanismen der Virusmorphogenese bei Retroviren und schloss sich als Postdoc der Gruppe von Professor Ralf Bartenschlager am Institut für Virologie in Mainz an. 2002 wechselte er gemeinsam mit Bartenschlager an die Abteilung für Molekulare Virologie der Universität Heidelberg. Dort etablierte Thomas Pietschmann eine Emmy Noether-Nachwuchsgruppe, die sich mit der Morphogenese und dem Eintrittsmechanismus des Hepatitis-C-Virus beschäftigte. Im Frühjahr 2007 wurde er mit seiner Arbeitsgruppe an das TWINCORE berufen und leitet dort seit 2012 das Institut für Experimentelle Virologie. Seit 2021 ist er Sprecher des Helmholtz Forschungsprogramms „Infektionsforschung" am HZI und ist seit 2023 Vorstandsmitglied des Deutschen Zentrums für Infektionsforschung (DZIF) und Prokurist für die Wissenschaftliche Geschäftsführung des HZI.
Ausgewählte Publikationen
Sake SM, Zhang X, Rajak MK, Urbanek-Quaing M, Carpentier A, Gunesch AP, Grethe C, Matthaei A, Rückert J, Galloux M, Larcher T, Le Goffic R, Hontonnou F, Chatterjee AK, Johnson K, Morwood K, Rox K, Elgaher WAM, Huang J, Wetzke M, Hansen G, Fischer N, Eléouët JF, Rameix-Welti MA, Hirsch AKH, Herold E, Empting M, Lauber C, Schulz TF, Krey T, Haid S, Pietschmann T. Drug repurposing screen identifies lonafarnib as respiratory syncytial virus fusion protein inhibitor. Nat Commun. 2024 Feb 8;15(1):1173. doi: 10.1038/s41467-024-45241-y. PMID: 38332002; PMCID: PMC10853176.
Weber T, Potthoff J, Bizu S, Labuhn M, Dold L, Schoofs T, Horning M, Ercanoglu MS, Kreer C, Gieselmann L, Vanshylla K, Langhans B, Janicki H, Ströh LJ, Knops E, Nierhoff D, Spengler U, Kaiser R, Bjorkman PJ, Krey T, Bankwitz D, Pfeifer N, Pietschmann T, Flyak AI, Klein F. Analysis of antibodies from HCV elite neutralizers identifies genetic determinants of broad neutralization. Immunity. 2022 Feb 8;55(2):341-354.e7. doi: 10.1016/j.immuni.2021.12.003. Epub 2022 Jan 5.
Risso-Ballester J, Galloux M, Cao J, Le Goffic R, Hontonnou F, Jobart-Malfait A, Desquesnes A, Sake SM, Haid S, Du M, Zhang X, Zhang H, Wang Z, Rincheval V, Zhang Y, Pietschmann T, Eléouët JF, Rameix-Welti MA, Altmeyer R. A condensate-hardening drug blocks RSV replication in vivo. Nature. 2021 Jul;595(7868):596-599. doi: 10.1038/s41586-021-03703-z. Epub 2021 Jul 7. PMID: 34234347.
Bankwitz D, Bahai A, Labuhn M, Doepke M, Ginkel C, Khera T, Todt D, Ströh LJ, Dold L, Klein F, Klawonn F, Krey T, Behrendt P, Cornberg M, McHardy AC, Pietschmann T. Hepatitis C reference viruses highlight potent antibody responses and diverse viral functional interactions with neutralising antibodies. Gut. 2021 Sep;70(9):1734-1745. doi: 10.1136/gutjnl-2020-321190. Epub 2020 Dec 15.
Bankwitz D, Doepke M, Hueging K, Weller R, Bruening J, Behrendt P, Lee JY, Vondran FWR, Manns MP, Bartenschlager R, Pietschmann T. Maturation of secreted HCV particles by incorporation of secreted ApoE protects from antibodies by enhancing infectivity. J Hepatol. 2017 Sep;67(3):480-489. doi: 10.1016/j.jhep.2017.04.010. Epub 2017 Apr 22.
Weitere Publikationen finden Sie hier.
Technologieangebote
Folgende Technologien wurden von der Abteilung Experimentelle Virologie entwickelt und zum Patent angemeldet:





