Antimikrobielle Wirkstoffe durch chemoenzymatische Synthese

Unsere Forschung
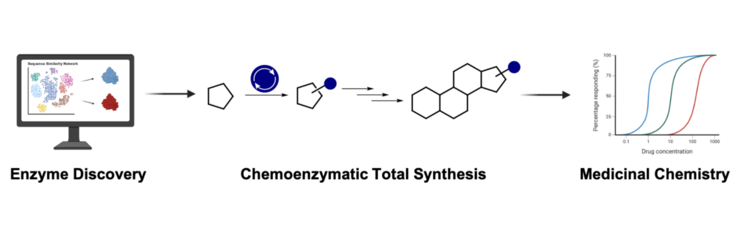
Naturstoffe (NPs) haben in der Vergangenheit eine entscheidende Rolle bei der Entdeckung von Medikamenten gespielt, da sie eine hohe Bioaktivität aufweisen und als wertvolle Vorlagen für therapeutische Wirkstoffe dienen. Ihr Einsatz in der Arzneimittelentwicklung hat jedoch abgenommen, vor allem wegen der Schwierigkeiten, die mit der Isolierung dieser Verbindungen aus natürlichen Quellen verbunden sind, oder wegen der Grenzen herkömmlicher synthetischer Methoden. Durch die Nutzung der einzigartigen Reaktivität und Selektivität von Enzymen aus NP-Biosynthesewegen in Kombination mit modernsten Techniken der organischen Chemie wollen wir praktische Lösungen für den Zugang zu diesen NPs und ihren Analoga entwickeln. Neben der Entwicklung praktikabler synthetischer Routen für Naturstoffe, die gegen Plasmodium falciparum, den Erreger von Malaria, Mycobacterium tuberculosis und andere Mikroorganismen wirksam sind, konzentrieren wir uns auf die Entdeckung neuartiger Biokatalysatoren. Durch die Erstellung einer Biokatalysatorbibliothek möchten wir das traditionelle synthetische Instrumentarium für die NP-Synthese verstärken und gleichzeitig tiefere Einblicke in die bisher wenig erforschte Enzymchemie geben.
Unsere Forschung
Naturstoffe (NPs) haben in der Vergangenheit eine entscheidende Rolle bei der Entdeckung von Medikamenten gespielt, da sie eine hohe Bioaktivität aufweisen und als wertvolle Vorlagen für therapeutische Wirkstoffe dienen. Ihr Einsatz in der Arzneimittelentwicklung hat jedoch abgenommen, vor allem wegen der Schwierigkeiten, die mit der Isolierung dieser Verbindungen aus natürlichen Quellen verbunden sind, oder wegen der Grenzen herkömmlicher synthetischer Methoden. Durch die Nutzung der einzigartigen Reaktivität und Selektivität von Enzymen aus NP-Biosynthesewegen in Kombination mit modernsten Techniken der organischen Chemie wollen wir praktische Lösungen für den Zugang zu diesen NPs und ihren Analoga entwickeln. Neben der Entwicklung praktikabler synthetischer Routen für Naturstoffe, die gegen Plasmodium falciparum, den Erreger von Malaria, Mycobacterium tuberculosis und andere Mikroorganismen wirksam sind, konzentrieren wir uns auf die Entdeckung neuartiger Biokatalysatoren. Durch die Erstellung einer Biokatalysatorbibliothek möchten wir das traditionelle synthetische Instrumentarium für die NP-Synthese verstärken und gleichzeitig tiefere Einblicke in die bisher wenig erforschte Enzymchemie geben.
Alexander Kiefer
Mit der unübertroffenen Kraft enzymatischer Reaktionen werden wir die Entdeckung von Arzneimitteln auf Basis natürlicher Produkte beschleunigen.
Nach Abschluss seiner Promotion unter der Leitung von Prof. Uli Kazmaier an der Universität des Saarlandes hat Alexander seine Fähigkeiten sowohl in der klassischen Totalsynthese als auch in der medizinischen Chemie verfeinert, um Cyclomarine mit verbesserten antimikrobiellen Aktivitäten zu erhalten. Während seines kurzen Postdoc-Aufenthalts an der Aalto-Universität in Finnland unter der Leitung von Prof. Dr. Jan Deska wechselte er von der klassischen Totalsynthese zur chemoenzymatischen Synthese und konzentrierte sich dabei auf das strukturell einzigartige Angiopterlacton B. Er entwickelte erfolgreich eine effiziente chemo-inspirierte biokatalytische Totalsynthese, die native enzymatische Substratumwandlung mit künstlichen Modulen mit abiotischen Transformationen integriert. Nachdem er Mitte 2019 in das Labor von Prof. Dr. Anna Hirsch am Helmholtz-Institut für Pharmazeutische Forschung Saarland (HIPS) wechselte, war er an einer Vielzahl von Forschungsprojekten im Bereich der medizinischen Chemie beteiligt. Mit Unterstützung des DFG-Walter-Benjamin-Programm-Stipendiums wechselte er Anfang 2022 in das Labor von Prof. Dr. Ben Shen in Scripps Florida, wo er als Projektleiter ein interdisziplinäres Team aus drei verschiedenen Labors leitete. Seine Forschungsbemühungen konzentrierten sich auf die Entwicklung von Anthrachinon-fusionierten Enedin-basierten Antikörper-Wirkstoff-Konjugaten als vielversprechende Antikrebsmittel. Nach seiner Rückkehr an das HIPS Mitte 2024 im Rahmen eines DFG-Walter-Benjamin-Rückkehrstipendiums wurde ihm der prestigeträchtige 21. Helmholtz-Investigator-Groups-Grant verliehen. Dies ermöglichte es ihm, seine Forschungsgruppe aufzubauen, die sich auf naturstoffinspirierte Wirkstoffentwicklung an der Schnittstelle von Chemie und Biologie konzentriert.
Ausgewählte Publikationen
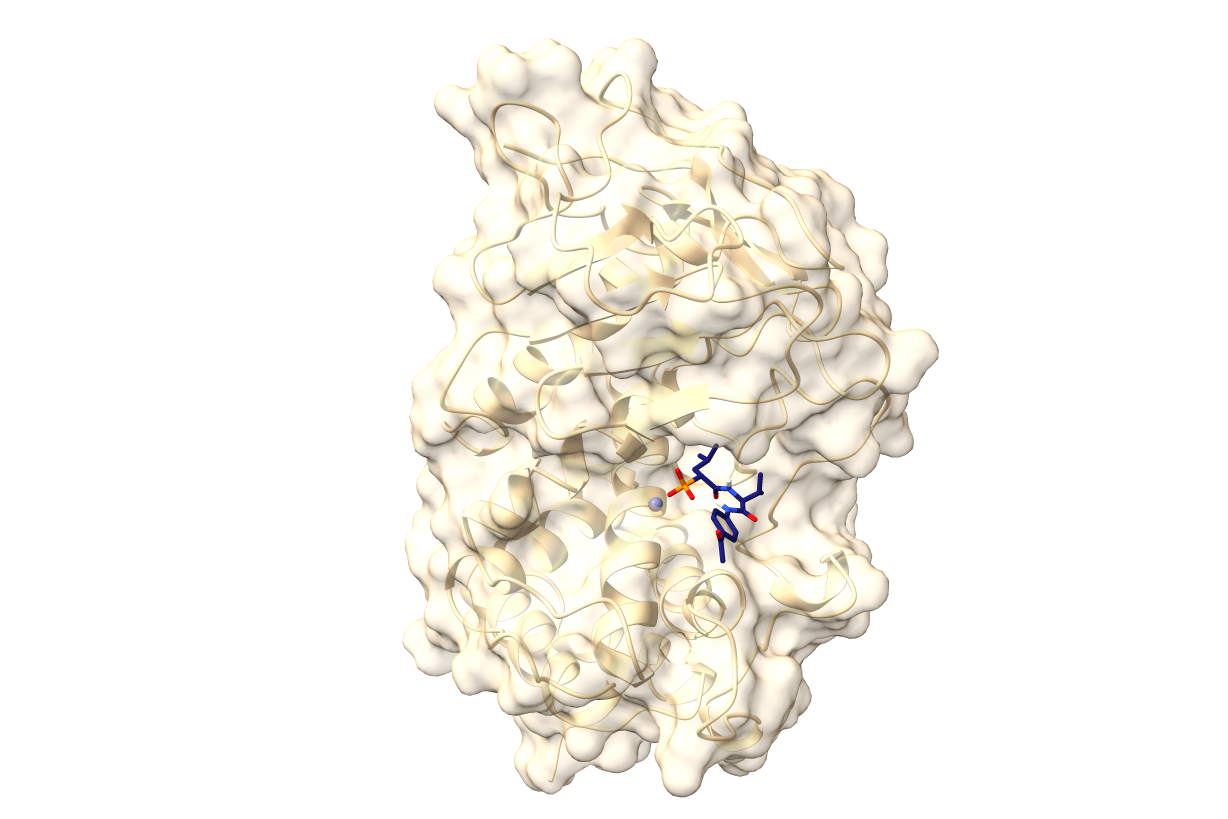
Alexander F. Kiefer*, Christian Schütz*, Colya N. Englisch, Dominik Kolling, Samira Speicher, Andreas M. Kany, Roya Shafiei, Noran A. Wadood, Ahmad Aljohmani, Niklas Wirschem, Ravindra P. Jumde, Andreas Klein, Asfandyar Sikandar, Yu-Mi Park, Gabriela Krasteva-Christ, Daniela Yildiz, Ahmed S. Abdelsamie, Katharina Rox, Jesko Köhnke, Rolf Müller, Markus Bischoff, Jörg Haupenthal and Anna K. H. Hirsch: "Dipeptidic Phosphonates: Potent Inhibitors of Pseudomonas aeruginosa Elastase B Showing Efficacy in a Murine Keratitis Model", Advanced Science 2024, 2411807. DOI: 10.1002/advs.202411807
Alexander F. Kiefer,* Yu-Chang Liu,* Rebecca Gummerer, Christina Jäger and Jan Deska: "An Artificial In Vitro Metabolism to Angiopterlactone B Inspired by Traditional Retrosynthesis", Angew. Chem. Int. Ed. 2023, 62, e202301178. DOI: 10.1002/anie.202301178
Andrew D. Steele,* Alexander F. Kiefer,* Dobeen Hwang,* Dong Yang, Christiana N. Teijaro, Ajeeth Adhikari, Christoph Rader, and Ben Shen: "Application of a Biocatalytic Strategy for the Preparation of Tiancimycin-based Antibody-Drug Conjugates Revealing Key Insights into Structure-Activity Relationships", Journal of Medicinal Chemistry 2023, 66, 1562–1573. DOI: 10.1021/acs.jmedchem.2c01771
Alexander F. Kiefer,* Spyridon Bousis,* Mostafa M. Hamed,* Eleonora Diamanti, Jörg Haupenthal and Anna K. H. Hirsch: "Structure-Guided Optimization of Small-Molecule Folate Uptake Inhibitors Targeting the Energy-Coupling Factor Transporters", Journal of Medicinal Chemistry2022, 65, 8869–8880. DOI: 10.1021/acs.jmedchem.1c02114
Alexander F. Kiefer, Chantal D. Bader, Jana Held, Anna Esser, Ran Rybniker, Martin Empting, Rolf Müller and Uli Kazmaier: "Synthesis of New Cyclomarin Derivatives and Their Biological Evaluation towards Mycobacterium Tuberculosis and Plasmodium Falciparum", Chem. Eur. J. 2019, 25, 8894–8902. DOI: 10.1002/chem.201901640
Publikationen
Eine vollständige Liste der Publikationen finden Sie auf der Webseite des HIPS.