Die Entdeckung antimikrobieller Wirkstoffe – wie etwa konventioneller Antibiotika – hat die Medizin verändert und ermöglicht, Infektionen zu behandeln, die zuvor als unheilbar galten. Allerdings ist die Entwicklung neuer Substanzen ins Stocken geraten, während unter anderem die unsachgemäße Gabe von Antibiotika die Entstehung von Resistenzen begünstigt. Daher besteht ein ständig wachsender Bedarf an neuartigen Methoden zur Bekämpfung von Krankheitserregern.
Antimikrobielle Wirkstoffe der Zukunft
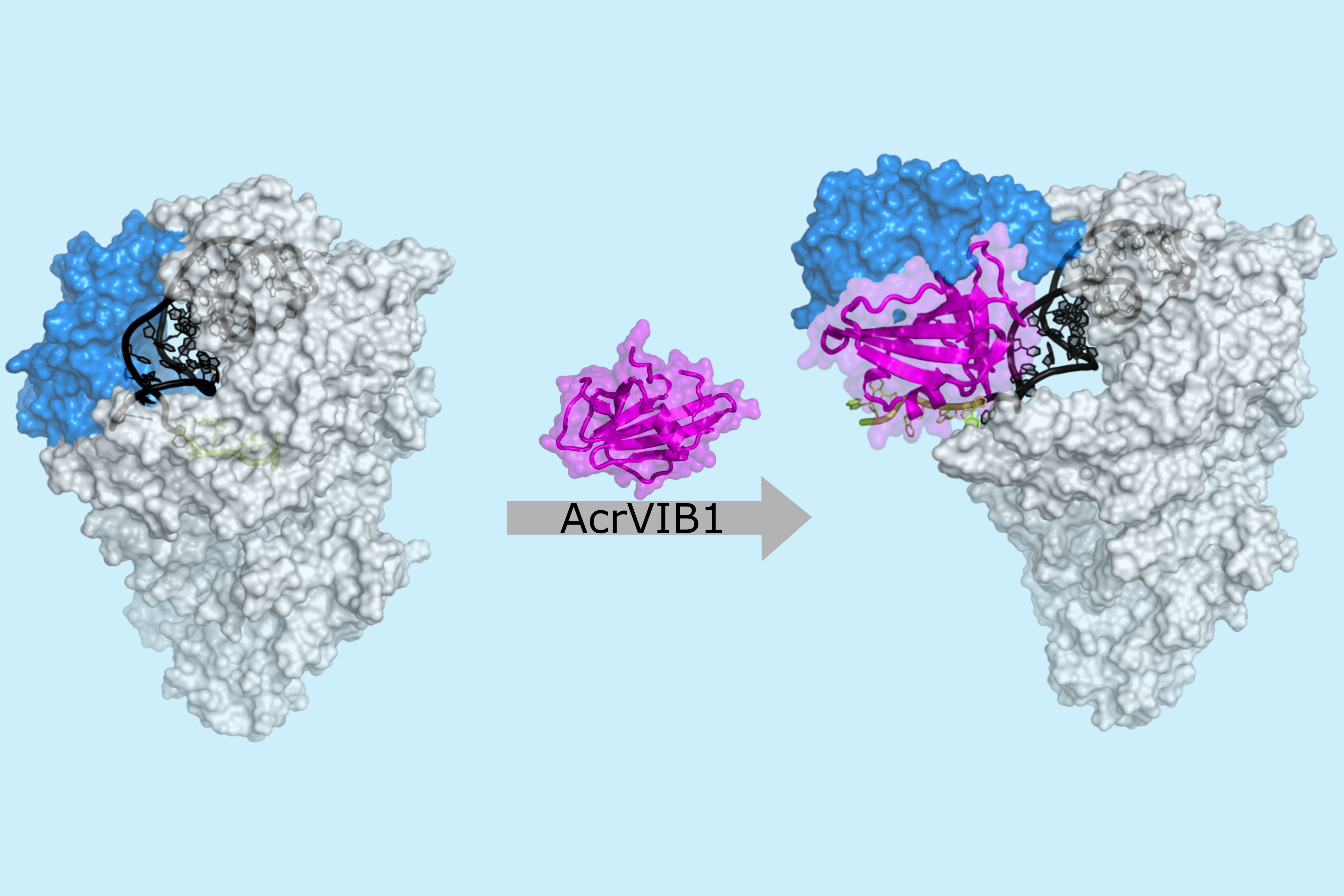
CRISPR-Cas-Systeme sind Bestandteil bakterieller Immunmechanismen, mit denen sich Bakterien gegen virale Invasionen wehren. Durch Umprogrammierung lassen sie sich auch für andere Zwecke einsetzen, zum Beispiel um Infektionen zu behandeln. Denn die Systeme können Mikroben allein auf der Basis von Gensequenzen gezielt abtöten. Bisher fehlten jedoch systematische Studien, um die Wirksamkeit der CRISPR-Antimikrobiotika zu bewerten, insbesondere für verschiedene Nukleasen, Angriffspunkte und Bakterienstämme. Um diese Lücke zu schließen, hat ein internationales Team unter Leitung des Helmholtz-Instituts für RNA-basierte Infektionsforschung (HIRI), einem Standort des Braunschweiger Helmholtz-Zentrums für Infektionsforschung (HZI) in Kooperation mit der Julius-Maximilians-Universität Würzburg (JMU), nun die erste umfassende Untersuchung dieser neuartigen Wirkstoffe durchgeführt. Im Mittelpunkt der Forschungsarbeit stand Klebsiella pneumoniae, eines der sogenannten ESKAPE-Bakterien. Die Abkürzung steht für eine Gruppe von Keimen, die gegen mehrere Antibiotika resistent sind.
„Klebsiella pneumoniae eignet sich besonders gut für eine Fallstudie, da es über viele Stämme mit unterschiedlichen Virulenz- und Resistenzeigenschaften verfügt“, sagt Chase Beisel, Leiter der Abteilung Synthetische RNA-Biologie am HIRI und Professor an der Medizinischen Fakultät der JMU. Er hat die internationale Studie in Zusammenarbeit mit Forschenden des Institut Pasteur in Paris, Frankreich, der Tel Aviv University in Israel, des HZI und der University of Toronto in Kanada koordiniert. Das Team aus vier verschiedenen Ländern vereinte die für eine Forschungsarbeit dieser Größenordnung erforderliche Expertise in den Bereichen CRISPR-Technologien, Klebsiella-Keime, Wirkstoffverabreichung mittels Bakteriophagen, Hochdurchsatz-Screening und maschinelles Lernen. Die Ergebnisse wurden heute in der Fachzeitschrift Nucleic Acids Research veröffentlicht.
Anderer Stamm, (manchmal) andere Wirkung
CRISPR-Cas-Systeme nutzen einen ausgeklügelten Verteidigungsmechanismus: Eine CRISPR-Ribonukleinsäure (RNA, von engl. ribonucleic acid) hilft dabei, Bereiche eines fremden Genoms, DNA oder RNA, zu erkennen. Anschließend zerschneidet die CRISPR-assoziierte Nuklease (Cas) ihr Ziel wie eine molekulare Schere. Die Wissenschaftler:innen konnten feststellen, dass verschiedene CRISPR-Nukleasen unterschiedlich effektiv sind. In ihren Experimenten zeigten Nukleasen, die auf DNA abzielen, eine bessere Leistung als solche, die RNA abbauen.
Darüber hinaus waren verschiedene Stämme von K. pneumoniae unterschiedlich empfindlich gegenüber bestimmten CRISPR-Antimikrobiotika, obwohl identische Nukleasen für die gleichen Angriffspunkte verwendet wurden. Elena Vialetto, Erstautorin der Studie und ehemalige Doktorandin in Beisels Labor, kommentiert: „Die variierende antimikrobielle Aktivität zwischen verwandten Stämmen war überraschend, wenn man bedenkt, dass wir die gleichen CRISPR-Konstrukte verwendet haben. Wir führen diesen Unterschied auf die Faltung der CRISPR-RNAs zurück, welche das DNA-Targeting, also die gezielte Veränderung eines Gens, steuern.“ Chase Beisel fügt hinzu: „Diese Studie zeigt erstmals, dass die antibakterielle Wirkung selbst zwischen verwandten Stämmen variieren kann.“
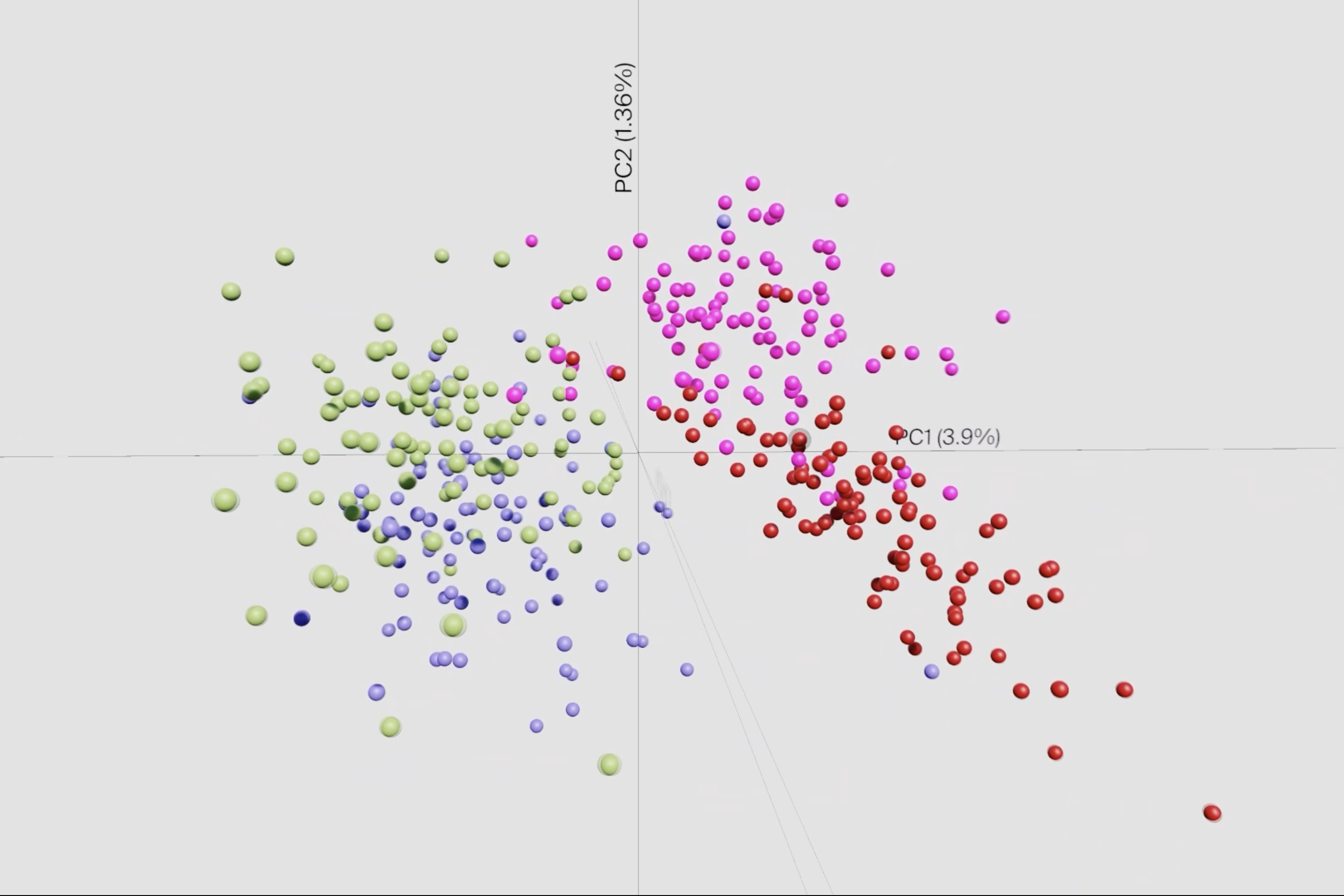
Um Merkmale zu identifizieren, die das Targeting in verschiedenen Stämmen verbessern könnten, führten die Forschenden ein genomweites Screening durch. Sie durchsuchten also alle Gensequenzen verschiedener K. pneumoniae-Stämme. Dabei haben sie Prinzipien und Parameter für das Design potenzieller antimikrobieller CRISPR-Wirkstoffe identifiziert und einen Algorithmus zur Vorhersage ihrer Effizienz trainiert.
Phagen als Trojanische Pferde
Außerdem wagte sich das Team an den nächsten Schritt in der Wirkstoffforschung, den Transport: Als Vehikel für die CRISPR-Antimikrobiotika nutzten die Wissenschaftler:innen Bakteriophagen, welche sie mit modifizierten Oberflächenmolekülen ausgestattet haben, um das Spektrum der Zielorganismen für die CRISPR-Fracht zu erweitern.
Diese Studie legt den Grundstein für die weitere Entwicklung von CRISPR als Werkzeug zur Vorbeugung oder Behandlung von Infektionen mit antibiotikaresistenten Erregern. „Wir hoffen, dass diese Arbeit den Einsatz von CRISPR als maßgeschneidertes antimikrobielles Mittel im Kampf gegen Antibiotikaresistenzen noch weiter in den Fokus rückt“, sagt Beisel abschließend.
Förderung
Die Studie wurde gefördert von der Joint Programming Initiative on Antimicrobial Resistance, dem Bayerischen Staatsministerium für Wissenschaft und Kunst über das Forschungsnetzwerk bayresq.net und dem Europäischen Forschungsrat (Grant an Udi Qimron).
Originalpublikation
Vialetto E, Miele S, Goren MG, Yu J, Yu Y, Collias D, Beamud B, Osbelt L, Lourenço M, Strowig T, Brisse S, Barquist L, Qimron U, Bikard D, Beisel CL: Systematic interrogation of CRISPR antimicrobials in Klebsiella pneumoniae reveals nuclease-, guide- and strain-dependent features influencing antimicrobial activity. Nucleic Acids Research (2024); DOI: 10.1093/nar/gkae281