Yersinia pseudotuberculosis ist ein Bakterium, das Lebensmittelvergiftungen verursacht. Es ist ein naher Verwandter von Yersinia pestis, dem Erreger der Pest. Um Krankheiten zu verursachen, verwendet die Spezies unter anderem ein Toxin, das aufgrund seiner Fähigkeit, in der Haut Nekrosen zu verursachen, zytotoxischer nekrotisierender Faktor (englisch: cytotoxic necrotizing factor (CNF)) genannt wird. Mehrere krankheitserregende Stämme von Escherichia coli produzieren ebenfalls CNF. „Obwohl verschiedene pathogene Spezies es verwenden, ist wenig über die dreidimensionale Struktur von CNF bekannt. Daher fehlt ein detailliertes Verständnis der Mechanismen, über die CNF Wirtszellen schädigt“, sagt Prof. Wulf Blankenfeldt, Leiter der Abteilung „Struktur und Funktion der Proteine“ am HZI. Das bremst sowohl die Entwicklung von Medikamenten, die CNF hemmen könnten, als auch die translationale Nutzung von CNF-Bestandteilen für biomedizinische Anwendungen aus.
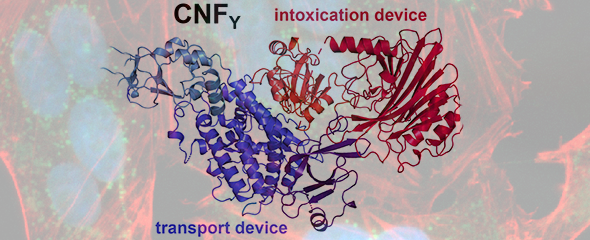
In der aktuellen Studie arbeitete Blankenfeldt mit mehreren Arbeitsgruppen des HZI und der ehemaligen HZI-Gruppenleiterin Prof. Petra Dersch, jetzt an der Universität Münster, zusammen, um die dreidimensionale Struktur von CNF aus Y. pseudotuberculosis zu bestimmen. Die Wissenschaftler zerlegten CNF in kleinere Teile, um das komplette Toxin sichtbar machen zu können. Sie fanden heraus, dass CNF aus fünf miteinander verbundenen Bausteinen besteht. „Als Strukturbiologen vergleichen wir normalerweise die Proteinstrukturen, die wir finden, mit einer oder mehreren der über 170.000 Strukturen, die bereits zuvor gelöst wurden und die im Internet frei verfügbar sind. Das war bei CNF nicht der Fall: Nur die Struktur des allerletzten Bausteins war vor etwa 20 Jahren untersucht worden. Es war nicht einmal klar, dass der Rest von CNF vier weitere Struktureinheiten enthält“, sagt Blankenfeldt. Die von seinem Team vorgestellte CNF-Struktur kann nun als Blaupause dienen, um Hemmstoffe zu entwickeln, die das Toxin neutralisieren.
Um Krankheiten zu verursachen, müssen Bakterien Toxine und andere molekulare Waffen an die richtige Stelle im Wirt bringen. Die Forscher entdeckten, dass die ersten drei Bausteine zusammen eine Transportvorrichtung bilden, die den toxischen Teil des CNF in die Zelle bringt. Ohne die eingebaute Liefervorrichtung können die beiden Bausteine, die das toxische Segment des Proteins bilden, nicht funktionieren, da sie in einem Zellkompartiment namens Endosom stecken bleiben. So kann das Toxin die Moleküle nicht erreichen, mit denen es interagiert, um die Zelle zu töten. „Viele Bakterien verwenden Toxine, die in die Wirtszelle transportiert werden müssen. Daher könnten unsere Ergebnisse auch Einblicke in die molekularen Mechanismen anderer Toxine geben“, sagt Blankenfeldt. Außerdem sieht er eine mögliche Anwendung der CNF-Transportmaschinerie für neuartige proteinbasierte Medikamente. Mit dem Wissen über die Liefervorrichtung können therapeutische Proteine an den CNF-Transportapparat gekoppelt werden, um sie dann ins Innere von Zellen zu bringen.
Originalpublikation:
Paweena Chaoprasid*, Peer Lukat*, Sabrina Mühlen*, Thomas Heidler, Emerich-Mihai Gazdag, Shuangshuang Dong, Wenjie Bi, Christian Rüter, Marco Kirchenwitz, Anika Steffen, Lothar Jänsch, Theresia E. B. Stradal, Petra Dersch# & Wulf Blankenfeldt#. Crystal structure of bacterial cytotoxic necrotizing factor CNFY reveals molecular building blocks for intoxication. EMBO J. Januar 2021. DOI: 10.15252/embj.2020105202 (* trugen zu gleichen Teilen bei, # korrespondierende Autoren)