RNA-Biologie eröffnet neue Wege zur Bekämpfung von Infektionen
Ribonukleinsäure, kurz RNA (von engl. ribonucleic acid), ist ein wahres Multitalent. Während die DNA als Bauplan des Lebens dient, ist RNA das vielseitige Werkzeug, das diesen Bauplan zum Leben erweckt. Dieses bemerkenswerte Molekül besteht aus den Nukleinbasen Adenin, Guanin, Cytosin und Uracil, die durch ein Zucker-Phosphat-Gerüst verbunden sind. Es sorgt dafür, dass Proteine hergestellt werden, dass zelluläre Prozesse reibungslos ablaufen und dass die Genexpression entsprechend den Bedürfnissen der Zelle reguliert wird. Dies gilt nicht nur für unsere eigenen Zellen, sondern auch für die unzähligen Krankheitserreger, denen wir täglich begegnen – von Bakterien wie Salmonellen und Escherichia coli bis hin zu Viren wie SARS-CoV-2 oder Influenza. Die RNA-Zusammensetzung einer Zelle liefert eine Momentaufnahme ihres Zustands in Echtzeit, egal ob gesund oder von Krankheit betroffen. Dank neuester technologischer Fortschritte können Forschende diesen „RNA-Expressionsatlas“ nun effizient bis auf die Ebene einzelner Zellen analysieren, was die Diagnose und das Verständnis von Krankheitsbildern erleichtert.
Auch für eine neuartige Form der RNA-basierten Medizin hat die Aufdeckung der vielfältigen Funktionen und Eigenschaften von RNA den Weg geebnet. Ob Infektionen, Krebs, Neurodegeneration, Stoffwechselstörungen oder seltene genetische Krankheiten – RNA verspricht neue Wege, um das Leben von Patient:innen zu verbessern und Krankheiten zu heilen. Ihre einzigartige Struktur und ihre biochemischen Eigenschaften machen sie zu einem idealen Ausgangsmaterial für die Herstellung von Medikamenten, Impfstoffen und biotechnologischen Werkzeugen. Denn wir beherrschen die Regeln der komplementären Basenpaarung, die das Bindungsverhalten und die Zielgenauigkeit der RNA bestimmen. Die rasche Entwicklung lebensrettender Boten-RNA-Impfstoffe gegen SARS-CoV-2 ist nur ein herausragendes Beispiel für die Innovationskraft von RNA in der modernen Medizin. „Die mRNA-Impfung gegen COVID-19 zeigt ganz deutlich, wie Wirkstoffe mit Ribonukleinsäuren sehr schnell entwickelt und spezifisch angepasst werden können. Diese Programmierbarkeit wollen wir uns zunutze machen, um neue maßgeschneiderte RNA-Therapeutika zu konzipieren und Infektionskrankheiten zu bekämpfen“, erklärt Jörg Vogel, Direktor des HZI-Standorts Helmholtz-Institut für RNA-basierte Infektionsforschung (HIRI) und Leiter der Abteilung „RNA-Biologie von bakteriellen Infektionen“.
Die Programmierbarkeit wollen wir uns zunutze machen, um neue maßgeschneiderte RNA-Therapeutika zu konzipieren und Infektionskrankheiten zu bekämpfen.

Basenabfolge als Schlüssel für RNA-Therapeutika
Für therapeutische Interventionen bietet die einzigartige Basenabfolge jedes RNA-Moleküls ein Angriffsziel für die Entwicklung von RNA-basierten Medikamenten. Im Gegensatz zur herkömmlichen Wirkstoffforschung, die ein aufwendiges Screening nach Leitsubstanzen erfordert, die mit Proteinen interagieren, können RNA-Therapeutika auf rationale Weise unter Verwendung etablierter Prinzipien der komplementären Basenpaarung entworfen werden. Zusammen mit den Fortschritten bei der Überwindung von zellulären Barrieren hat die RNA-Forschung ein enormes Potenzial, sowohl diagnostische Werkzeuge als auch therapeutische Strategien zur Behandlung von Krankheiten voranzubringen.
Eine vielversprechende Anwendung liegt im Kampf gegen die zunehmende Bedrohung durch antimikrobielle Resistenzen. Forschende am HIRI untersuchen den Einsatz von kurzen Antisense-Oligonukleotiden, die an bakterielle RNA binden und gezielt die Produktion von überlebenswichtigen Proteinen blockieren. Dieser programmierbare Ansatz ermöglicht es, resistente Bakterienstämme, Virulenzfaktoren oder neu auftretende Krankheitserreger gezielt zu bekämpfen und gleichzeitig das natürliche Mikrobiom zu schützen.
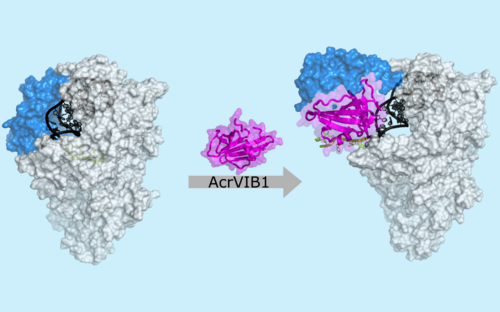
Ein weiteres bemerkenswertes Beispiel dafür, wie die RNA-Biologie Wissenschaft und Medizin verändert, ist die CRISPR-Cas-Technologie. Dieses revolutionäre Werkzeug, das auf einem natürlichen bakteriellen Abwehrmechanismus basiert, ermöglicht Wissenschaftler:innen die präzise Bearbeitung von Genen in lebenden Organismen. Mithilfe von RNA als Leitmolekül kann CRISPR-Cas spezifische DNA-Sequenzen ansteuern, um Gene zu schneiden, zu verändern oder zu ersetzen. Diese Technologie birgt ein enormes Potenzial für die Behandlung genetisch bedingter Krankheiten, die Bekämpfung bakterieller und viraler Infektionen und sogar die gesundheitsfördernde Modulation des menschlichen Mikrobioms.
Zusammenfassend lässt sich sagen, dass die RNA-Biologie bahnbrechende Fortschritte vorantreibt, die geeignet sind, Medizin und Biotechnologie zu revolutionieren und die globalen Gesundheitsherausforderungen unserer Zeit gezielt anzugehen.
(asp)
Stand: April 2025
Beteiligte Forschungsgruppen
-
Einzelzellanalyse
 Prof. Dr. Antoine-Emmanuel Saliba
Prof. Dr. Antoine-Emmanuel Saliba -
Genom-Architektur und Evolution von RNA-Viren
 Dr. Redmond Smyth
Dr. Redmond Smyth -
Integrative Informatik der Infektionsbiologie
 Prof. Lars Barquist
Prof. Lars Barquist -
Klinische Bioinformatik
 Prof. Dr. Andreas Keller
Prof. Dr. Andreas Keller -
Komplexe in Phageninfizierten Zellen
 Dr. Milan Gerovac
Dr. Milan Gerovac -
LncRNA und Infektionsbiologie
 Prof. Dr. Mathias Munschauer
Prof. Dr. Mathias Munschauer -
Molekulare Grundlagen von RNA-Phagen
 Jun.-Prof. Dr. Jens Hör
Jun.-Prof. Dr. Jens Hör -
Rekodierungsmechanismen in Infektionen
 Prof. Neva Caliskan
Prof. Neva Caliskan -
RNA-Biologie gram-positiver Bakterien
 Prof. Dr. Franziska Faber
Prof. Dr. Franziska Faber -
RNA-Biologie von bakteriellen Infektionen
 Prof. Dr. Jörg Vogel
Prof. Dr. Jörg Vogel -
Synthetische RNA-Biologie
 Prof. Dr. Chase Beisel
Prof. Dr. Chase Beisel -
Wirt-Pathogen-Mikrobiota Interaktionen
 Prof. Dr. Alexander Westermann
Prof. Dr. Alexander Westermann